동아ST, B형간염 치료제 ‘베믈리아’ 1주년…매출 확대 박차
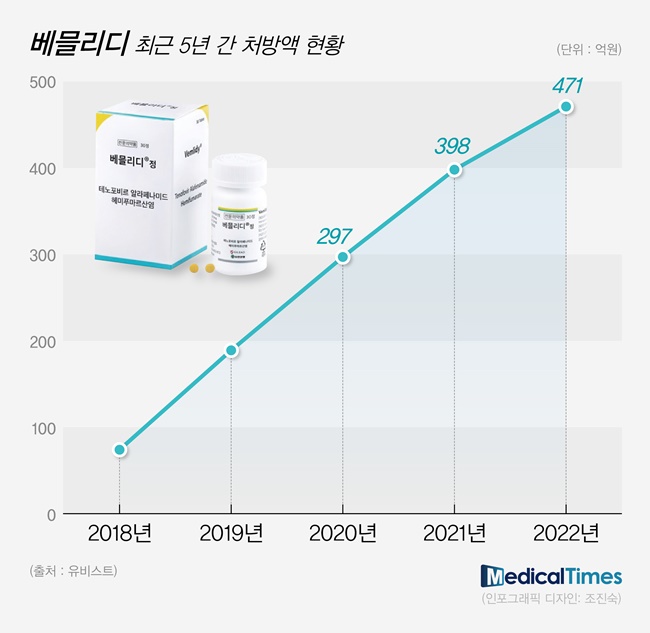
메디칼타임즈=허성규 기자동아에스티의 B형간염 치료제 '베믈리아'동아에스티(대표이사 사장 김민영)의 B형간염 치료제 ‘베믈리아(Vemlia)’가 출시 1주년을 맞아 본격적인 매출 확대에 나선다고 1일 밝혔다.베믈리아는 오리지널 의약품의 주성분인 테노포비르 알라페나미드 헤미푸마르산염(Tenofovir Alafenamide hemi-Fumarate)을 테노포비르 알라페나미드 시트르산염(Tenofovir Alafenamide Citrate)으로 변경했다.염 변경을 통해 오리지널 의약품 대비 용출률을 높이고 가혹환경에서 유연물질 발생을 감소시켰으며, 해당 내용으로 특허 출원했다.또한 오리지널 의약품 대비 약 27% 낮은 약가를 받아 환자들의 경제적 부담을 낮췄으며, 환자가 약통을 열고 닫을 때 마다 복용 요일 확인이 가능한 요일약통을 적용해 환자의 복약순응도를 높였다.특히 B형간염 환자와 의료진에게 보다 많은 신뢰를 줄 수 있도록 오리지널 의약품 대비 베믈리아의 비열등성을 입증하는 임상을 진행하고 있다.이러한 특장점으로 베믈리아는 출시 1년만에 전국 주요 상급종합병원을 비롯해 60여 개 종합병원에서 약사위원회를 통과한 만큼, 올해는 클리닉 시장과 함께 종합병원 시장의 처방 확대에도 집중할 계획이다.UBIST data 기준 테노포비르 알라페나미드 시장은 2022년 492억 원에서 지난해 약 600억 원대 규모로 성장했으며, 종합병원과 클리닉 시장의 매출 비중은 6대 4 이다.동아에스티 관계자는 "지난 1년간 베믈리아의 우수성을 적극 알리며 처방 확대의 기반을 닦는데 노력해 온 결과 타 염 변경 제품 대비 많은 종합병원에서 약사위원회를 통과했다"며 "올해는 B형 간염치료제 시장에서 베믈리아가 두각을 나타낼 수 있도록 영업과 마케팅을 집중하겠다"고 말했다.한편, 동아에스티는 베믈리아 외에도 헵세비어(Hepsevir, 성분명: Adefovir dipivoxil), 바라클(Baracle, 성분명: Entecavir), 비리얼(Virreal, 성분명: Tenofovir disoproxil orotate) 등 다양한 B형간염치료제 포토폴리오를 갖추고 있다.